Einleitung
In diesem Bericht wird erklärt, warum Schweratome, die in einem
Tumor eingelagert sind, bei der Strahlentherapie eine erhöhte
Herddosis bewirken: durch die Anreicherung eines Tumors mit
Schweratomen (z.B. Jod, Gold oder Platin) wird hier während
einer Hochvoltbestrahlung vermehrt die Bildung von Positronen
und Elektronen angeregt. Dadurch bedingt entsteht durch die
gegenseitige Vernichtung von Positron und Elektron die
so genannte Vernichtungsstrahlung mit der Energie von 0,511 MeV.
Diese Vernichtungsstrahlung löst nun im Tumor die auf kleinem
Raum (Millimeterbereich) ablaufenden
Compton-Photo-Komplexreaktionen aus, welche räumlich eng an die
Schweratome gebunden sind, d.h. bei einem hochenergetischen
Comptoneffekt mit einem Schweratom wird ein Elektronenschauer
frei, und die resultierende niederenergetische
Comptonstreustrahlung wird innerhalb einer mittleren Entfernung
von 2 mm neben dem Schweratom durch ein Leichtatom (z.B.
Sauerstoff, Kohlenstoff oder Stickstoff) mittels eines
Photoeffektes absorbiert. Auch die mittelenergetische
Comptonstreustrahlung (um 100 KeV) aus dem umgebenden Gewebe
wird zusätzlich mit hoher Incidenz proportional der 4. Potenz
der effektiven Ordnungszahl des Tumors im schweratombeladenen
Tumorgewebe durch Photoeffekte absorbiert. Mittelschwere Atome
wie Zink oder Eisen führen bei Anreicherung im Tumor zu einer
vermehrten Photoabsorption der mittel- und niederenergetischen
Comptonstreustrahlung aus dem Gewebe um den Tumor.
Schweratome im Tumor
Nunmehr wird
bei der Hochvolttherapie die Wirkung von Schweratomen in einem
Tumor zuerst theoretisch und dann an konkreten Beispielen
erörtert.
Hochenergetische Comptoneffekte
Schon vor
Jahrzehnten wurden in der Strahlenphysik (1, 2) die Grundlagen
für diesen neuen Ansatz in der Strahlentherapie erforscht,
welcher zum Ziel hat, möglichst viele schwere Atome selektiv in
ein Malignom einzubringen. Schweratome haben die Fähigkeit, aus
Hochvoltphotonen durch hochenergetische Comptoneffekte (1, 2)
sehr viel mehr Energie zu entnehmen, als dies bei leichten
Atomen möglich ist. Dabei werden aus einem Schweratom viele
Elektronen auf einmal freigesetzt, wodurch sich ein
beträchtlicher Energieanteil eines Hochvoltphotons verbraucht (1
, 2).
Sekundär- und
Tertiärelektronen
Diese
freigesetzten Elektronen setzen noch Sekundär- und
Tertiär-Elektronen frei (2) und stören und verändern die
biochemischen Bindungen in den Chromosomen, womit der Zelltod
verursacht wird. Die verbleibenden Comptonstreustrahlen werden
dann von Schweratomen hauptsächlich durch Photoeffekte (1 , 2)
absorbiert, wobei ebenfalls Elektronen freigesetzt werden,
welche zerstörend wirken.
Beziehung
Enhancement im CT <-> erhöhte Herddosis bei der Hochvolttherapie
Werte Leser,
ersparen Sie mir, an dieser Stelle Formeln für die zu erwartende
Wirkung anzuführen! Ich fand 1989 (6) Näherungen, welche
zeigten, dass die Wahrscheinlichkeit für Elektronenpaarbildung
(1, 2), Comptoneffekte und Photoeffekte bei Einlagerung von
Schweratomen in einen Tumor steigt und das dabei im CT erzielte
Enhancement zur Berechnung der zu erwartenden Herddosis
verwendet werden kann (6).
Höheres
Energieniveau der Einfallsstrahlung - größerer
Verstärkungseffekt durch Schweratome
Aber es ist
schwierig, Energieniveaus von 1 MeV aufwärts bis 25 MeV
stufenweise in die Formel einfließen zu lassen. Ebenso schwierig
ist das Einbeziehen von Sekundär- und Tertiärelektronen in diese
Formel. Auch die Ordnungszahl der verwendeten Schweratome spielt
eine größere Rolle, als erwartet (3, 4).
In Zukunft
sollten wir uns lieber von der Empirie führen lassen. In
Wirklichkeit scheinen die Effekte viel stärker zu sein, als die
von mir damals errechneten (3, 4, 5, 8).
Compton-Photo-Komplexreaktionen
Wenn bei
hochenergetischen Comptoneffekten niederenergetische
Comptonstreustrahlen frei werden und im Umkreis von zwei
Millimetern wieder absorbiert werden, so kann man diesen Vorgang
als Compton-Photo-Komplexreaktion bezeichnen (6).
Eisenpigment führte zur selektiven Zerstörung des Astrocytoms IV
Durch solche
Compton-Photo-Komplexreaktionen wurde vor 8 Jahren ein junger
Mann, der an einem Astrocytom IV im Hirnstamm erkrankt war,
geheilt. Bei ihm war es durch Einblutungen zu einer starken
Eisenpigmentansammlung im Tumor gekommen. Die von mir
veranlasste
Strahlentherapie mit Kobalt 60 führte bei einer verabreichten
Herddosis von nur 50 Gy zur völligen Zerstörung des Tumors.
Ähnliche Effekte könnte man jederzeit mit Hilfe von
Jodkontrastmittel, wie man es beim CCT verwendet, beim
Astrocytom, beim Meningeom und beim Neurinom im Hirnschädel
erzielen, wenn man eine Stunde vor einer One- Shot- Therapie mit
20 Gy das Kontrastmittel i.v. verabreicht. Diese Tumoren zeigen
nämlich beim CCT ein Enhancement von bis zu 20
Hounsfield- Einheiten, was durch die eingelagerten Jodatome
verursacht wird.
Absolute
Todeskandidaten schon morgen heilbar
Am Astrocytom
IV leidende absolute Todeskandidaten könnten schon ab morgen
geheilt werden, wenn man diesen höchst einfachen Schritt in die
Zukunft wagen würde. Untermauert wird diese Behauptung durch
Arbeiten aus Amerika (3, 4) mit einer großen Anzahl von
Patienten, welche vom Radiosensitizing mit Bromdesoxyuridin
(BDU) und Joddesoxyuridin (JDU) berichten. Jod im JDU ist
wesentlich schwerer als Brom im BDU. Jod hat in seiner Hülle 53
Elektronen, Brom nur 35 (1). Jod kann daher mehr Elektronen
abgeben, wenn ein Hochvoltphoton "einschlägt"(1).
Obwohl JDU und
BDU sich biochemisch gleich verhalten, kommt es beim Astrocytom
IV mit JDU als Radiosensitizer zu Zweijahresüberlebensquoten von
68%, beim BDU aber von nur 28%. Man bedenke aber, dass bei diesen
Substanzen noch kein Enhancement im CT erkennbar ist. Deshalb
braucht man für diese Effekte noch 60 Gy Herddosis.
Cisplatin als Radiosensitizer
Im HNO-Bereich
bei fortgeschrittenen Carcinomen wurde in Amerika bei 68
Patienten Cisplatin als Radiosensitizer verwendet (5) und damit
eine Zweijahresüberlebensrate von 53% und eine
Fünfjahresüberlebensrate von 32 % erzielt. Platin hat 78
Elektronen in seiner Hülle und führt damit zu diesen
erstaunlichen Ergebnissen.
sichtbares
Enhancement - sichere Zerstörung des Tumors
Aber bei einem
jodbedingten sichtbaren Enhancement von 20 Hounsfieldeinheiten
wie beim CCT eines Astrocytoms IV wird man mit einer wesentlich
geringeren Herddosis auskommen, wobei man aber eine völlige
Zerstörung des Tumors erzielt.
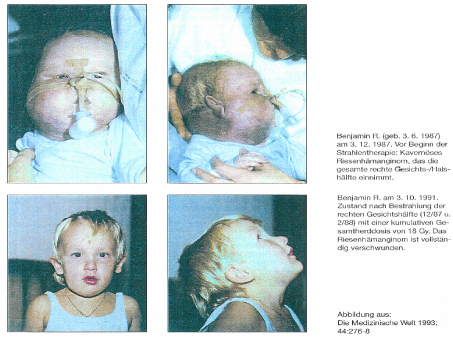
Professor Pfab in Marburg an der Lahn erzielte bei einem
cavernösen Riesenhämangiom (8) im Kopf- und Halsbereich mit
einer Einfallsdosis von nur 18 Gy mit harten Photonen der
Energie von 10 MeV ein völliges Verschwinden des Tumors. In
Lissabon wurden cavernöse Leberhämangiome mit Herddosen von nur
20 bis 30 Gy mit Telekobalt gestoppt (9). Diese Effekte werden
durch Eisen, welches als mittelschweres Atom der Ordnungszahl 26
sehr massiv in den Erythrocyten des strömenden Blutes der Hämangiome
vorhanden ist, durch hochenergetische Comptoneffekte erzielt.
Die Elektronen schädigen die Gefäßwände, bevor sie vom Eisen
wieder eingefangen werden, was zum Verschwinden des Hämangioms
oder zumindest zum Aussetzen des Wachstums führt.
Radiosensitizing mit Kupfer und Selen
Vor
fünfeinhalb Jahren wurde bei einem Patienten wegen eines Plattenepithelkarzinoms an der Epiglottis die Epiglottis entfernt.
Danach erhielt er eine Telekobalttherapie mit einer Herddosis
von 60 Gy. Ich verordnete als Radiosensitizer während der
Bestrahlung die Einnahme von Kupfer-Selen- Trinkampullen, jeden
zweiten Tag eine Ampulle. Er nahm sie auch noch Monate nach der
Strahlentherapie ein und ist bis jetzt frei von Rezidiven. Selen
hat 34 Elektronen, Kupfer 29 Elektronen in der Atomhülle. Bei
Darm- und Mammakarzinomen beobachtet man eine gute Aufnahme und
Speicherung von verabreichtem Selen in den Krebszellen. Ich
nehme an, da Plattenepithelkarzinome eine ähnliche Fähigkeit
besitzen. Jedenfalls sollte man ein Radiosensitizing mit
Kupfer-Selen versuchen, z.B. täglich eine Ampulle Kupfer-Selen,
um mögliche Chancen zu nutzen.
Überdosis des Selens würde den
Verstärkungseffekt vernichten
Wichtig ist
eine relativ niedrige Dosierung von Selen, damit nicht der
Charakter der selektiven Speicherung in den Tumorzellen durch
eine erzwungene Speicherung in normalen Körperzellen
verlorengeht, wenn man zu hoch dosiert.
Bei der
Bestrahlung von Plattenepithelkarzinomen im HNO-Bereich ergibt
sich folgendes Problem: Wird die Einfallsdosis der
Hochvoltbestrahlung größer als 30 Gy, so entsteht mit
zunehmender Dosis eine schmerzhafte Mukositis (7) und allmählich
auch eine Atrophie der Speicheldrüsen.
Schlussfolgerung:
In Zukunft
wird es nötig sein, einen so wirksamen Radiosensitizer zu
verwenden, dass mit einer Herddosis von nur 30 Gy die sichere
Zerstörung der Tumorzellen durch Hochvolttherapie erzielt wird.
Diese Forderung möchte ich auf sämtliche Tumoren ausdehnen,
welche mit der Strahlentherapie behandelt werden. Ich nehme an,
dass es durch diesen Bericht bald zu Fortschritten in diese
Richtung kommt.
Literatur;
(1)
Gerthsen-Kneser-Vogel:
Physik, Springer- Verlag
(2)
Theodor
Laubenberger:
Leitfaden der medizinischen Röntgentechnik, Diagnostik,
Dosimetrie, Strahlenschutz, Strahlentherapie, Deutscher
Ärzte-Verlag
(3)
C. Urtasun,
D. Cosmatos, J. Del Rowe, T. J. Kinsella, S. Lester, T.
Wasserman and D. S. Fulton:
Jododeoxyuridine (IdUR) combined with radiation in the treatment
of malignant glioma - a comparison of short versus long
intravenous dose schedules (RTOG 86-12)
(4)
H. S. Greenberg, W. F.
Chandler, W. D. Emsminger, H. Sandler, L. Junck, M. A Page, D.
Crane, P. McKeever, R. Tankanow and J. Bromberg:
Radiosensitisation with carotid intra-arterial bromodeoxyuridine
+ 5-fluoruracil biomodulation for malignant gliomas; Neurology,
Sept. 1994,441715
(5)
Prakash B.
Chougule, Steve Suk, Quyen D. Chu, Louis Leone, Peter T Nigri,
Robert McRae, Mary Lekas, Anthony Barone, Dinesh Bhat and Josef
Bellino:
Cisplatin as a Radiation Sensitizer in the Treatment of Advanced
Head end Neck Cancers; Cancer, Vol. 74, No.7, Oct.1, 1994
(6)
F.
Silberbauer:
Strahlentherapie mit erhöhter Wirksamkeit, Radiologe (1989) 29:
48-49
(7)
Doz. Dr. M.
Grasl, Univ. Klinik f. HNO- Krankheiten, Wien:
Schleimhaut-Irritationen bei Bestrahlung und Chemotherapie im
HNO-Bereich
(8)
H. Proske, R. Pfab:
Indikationsstellung zur Hochvoltbestrahlung kavernöser
Riesenhämangiome, eine eindrucksvolle Kasuistik, Die
Medizinische Welt 1993, 44:276-8
(9)
L.
Gaspar, F. Mascarenhas, M. Sa da Costa, J. Schaller Dias,
J. Gamma Alfonso, M. E. Silvestre: Radiation therapy in the
unresectable cavernous hemangioma of the liver, Radiotherapy and
Oncology 29 (1993) 45-50
zurück

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()